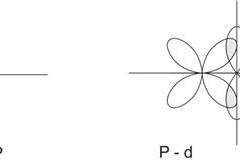МАТЕРИАЛЫ В АРМАТУРОСТРОЕНИИ. О МЕХАНИЗМЕ ХЛАДНОЛОМКОСТИ
Кривцов Ю.С., академик МАХ, Санкт-Петербург
Горобченко С.Л., к.т.н. Санкт-Петербург
ВВЕДЕНИЕ
С развитием криогенной технологии и ростом отрасли сжиженного природного газа определенно утвердился интерес к явлениям хладноломкости используемых материалов. Понимание процессов вязко-хрупкого перехода создает возможности и для лучшего понимания возможностей создания новых сталей и сплавов для криогенной арматуры.
В своей работе, проведенной в свое время в лаборатории криогенных сталей и сплавов ЛТИХП, Санкт-Петербург, мы предлагаем ознакомиться с воззрениями на теорию хладноломкости с точки зрения электронной теории металлов, способной дать ответы на многие вопросы специалистов – металловедов, работающих в арматурной отрасли.
ЭЛЕКТРОННАЯ ТЕОРИЯ ХЛАДНОЛОМКОСТИ
Ряд авторов (1-3) убедительно показал, что явление хладноломкости может быть связано с переходом металлической связи в более жесткую ковалентную. Поставим задачу: определить механизм перехода металлической связи в ковалентную при понижении температуры. Он может основываться на следующих представлениях (1):
-Атомы различных элементов имеют различную степень ионизации при образовании кристаллической решетки;
-Энергетические характеристики электронов, определяющих возможность их коллективизации с образованием металлической связи или гибридизации с образованием ковалентной связи, также различны.
Известно, что полная энергия кристалла складывается из нескольких составляющих:
Еполн=Е1+Е2+Е3+Е4 (1)
Где:
Е1 – энергия кулоновского взаимодействия между положительно заряженными ионами;
Е2 – энергия кулоновского взаимодействия между отрицательно заряженными электронами;
Е3 – энергия кулоновского взаимодействия между положительно заряженными ионами и отрицательно заряженными электронами;
Е4 – кинетическая энергия электронного газа.
Поскольку в решетке силы кулоновского взаимодействия между одноименными ионами и электронами примерно равны, т.е. решетка существует при некотором равновесном расстоянии между атомами r0 , то вся энергия кристалла определится как:
Е=Е3+Е4
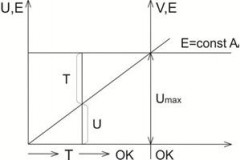
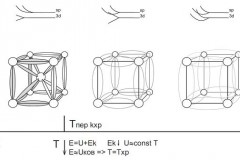
Вся энергия кристалла и все процессы, происходящие в нем, определяются через изменение соотношения кинетической и потенциальной энергии частиц, находящихся в кристалле. С понижением температуры доля кинетической энергии в общей энергии кристалла будет убывать, рис.1.
Рис. 1. Изменение соотношения кинетической и потенциальной энергии в кристалле при изменении температуры
При понижении температуры большая часть кинетической энергии перейдет в потенциальную, при этом полная энергия всегда остается величиной положительной. Для этого соотношения справедлива формула (2):
Е4+Ткин>0 (2)
Поскольку кинетическая энергия частиц кристалла не может быть величиной отрицательной, то должно существовать состояние при Т=Ткр, где большую часть процессов будет определять более «жесткая» потенциальная энергия, превышение которой должно привести к разрыву связей в элементарном объеме, и далее к разрушению кристалла.
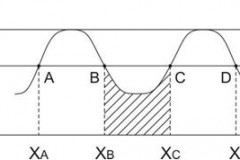
На графике движения это будет выглядеть как ограничение движения электрона определенным элементарным объемом. Движение электрона станет «финитным», т.е. ограниченным в пределах элементарной ячейки с длиной пробега не более параметра решетки. Электрон не сможет попасть из области ВС в область АВ, а в кристалле появляются разрешенные и запрещенные зоны, рис. 2.
Рис. 2. Изменение разрешенных движений электронов с понижением температуры
Из графика, рис .2 видно, что при снижении кинетической энергии, будет недостаточно энергии системы для попадания из одной области в другую. Термодинамически такое понимание процессов хладноломкости может быть связано с большим падением энергии «теплового» члена по сравнению с потенциальным.
F=U-TS ∆U < ∆ (TS) (3)
В связи с меньшим влиянием температуры на процессы электростатической и кулоновской связи большая часть изменения свободной энергии кристалла будет определяться «потенциальным» членом.
F = ∆U (4)
При этом наблюдаются такие эффекты, как возрастание электрических свойств металла при низких температурах, т.е. сверхпроводимость. Электрон не испытывает помех при движении под действием электрического тока из-за тепловых колебаний.
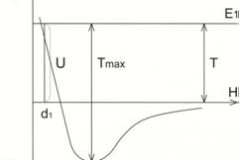
Этот эффект также соответствует уменьшению эффективного диаметра молекул – тому наименьшему расстоянию, до которого могут сблизиться атомы в момент соударения с повышением температуры. В момент соударения будет наблюдаться большее перекрытие электронных оболочек и больше электронов являются коллективизированными в момент соударения. Более сильная коллективная связь между электронами приведет к большей пластичности. При большей энергии Е2 эффективный диаметр d2 будет больше, чем d1 при меньшей энергии E1, рис. 3.
Рис. 3. Изменение энергии связи с понижением температуры
Процесс перехода кинетической энергии в потенциальную может быть хорошо описан и через изменение энергии электронов в сфере Ферми. Электронная концентрация вне сферы Ферми с понижением температуры будет уменьшаться, т.е. меньшее число электронов будет участвовать в создании металлической связи за счет коллективизированных электронов. Изменение энергии электронов по отношению к сфере Ферми в зависимости от температуры представлено на рис. 4.
f
Ef (T=0K) E
Рис. 4. Распределение электронов по энергиям в зависимости от температуры
В самом строении электронных оболочек будут происходить изменения. Из-за возрастания потенциального барьера стенки потенциальной ямы, в которой находится электрон в поле действия потенциальных сил, станут более вертикальными, рис.5, т.е. сузится количество возможных энергетических состояний электрона.
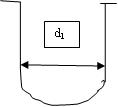
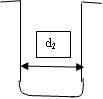
Т1 Т2
Рис. 5. Изменение потенциального барьера для прохода электронов с понижением температуры Т1>Т2
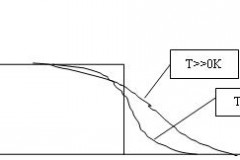
Это приведет к уменьшению количества подуровней с расщепленными зонами и как следствие, к уменьшению количества перекрываемых зон, рис.6. Изменение электронной концентрации по уровням при снижении температуры хорошо объясняется через изменения в строении 3d – SP оболочек при снижении температуры.
Хорошим примером является никель и железоникелевые сплавы. Феномен «инвара» появляется из-за гибридизации 3d-SP уровней, что создает эффект расширения сферы Ферми с сохранением значительного количества коллективизированных электронов с устойчивой связью в кристалле. В свою очередь это предотвращает переход к ионной и атомной ковалентной связи или координационной парной связи Вандер-Ваальса. Обеспечивается хорошее поддержание связей и «залечивание» решетки коллективизированными электронными облаками при растяжении.
А) Т>>0K
В) Т>0K
Рис. 6. Изменение зон разрешенных состояний подуровней с изменением температуры металлов
Такое понимание развития хладноломкости также объясняет, почему легирование никелем, как имеющего высокий уровень перекрытия электронных орбиталей, приводит к высокой пластичности одновременно для всех классов сталей, независимо от структуры: ферритных (0Н3А-0Н12А), аустенитных (12Х18Н10Т), и мартенситностареющих (07Х16Н6).
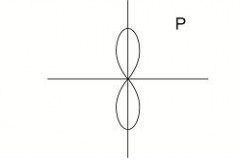
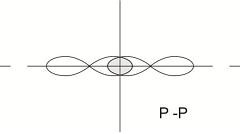
Сужение энергетически возможных состояний электрона при условии сохранения связей между ионным остовом и электронным облаком - это сосредоточение электронной плотности на определенных электронных орбиталях. Происходит вырождение равномерно распределенного электронного облака в определенные формы электронных облаков, соответствующих этим орбиталям. Фактически это будут орбитали s, p и d, рис. 7.
Рис. 7. Типы орбиталей: А) – S; Б) – p; В) - d
Поскольку условия сохранения кристалла требуют при неравномерном распределении электронной плотности концентрации ее вдоль прямых, соединяющих соседние ионы, то фактически это означает, что металлическая связь вырождается в ковалентную. Доля этой ковалентной составляющей с понижением температуры будет расти. Этим и объясняется эффект значительного повышения прочности с понижением температуры, поскольку ковалентная связь гораздо «жестче» и, соответственно, прочнее металлической.
Связь в кристалле будет осуществляться уже не совокупностью связей ионного остова и равномерно распределенного электронного облака, а направленным перекрытием электронных орбиталей. При этом способность металлов к сохранению пластических свойств, обеспечиваемых уровнем коллективизации электронов и степенью перекрытия электронных орбиталей, будет определяться особенностями σ или π – связей, рис. 8.
А) σ - связь
Б) π - связь
Рис. 8. Типы связей в кристалле с понижением температуры
Изменение состояния электронного облака в кристалле представлено на рис .9.
Рис.9. Изменение состояния электронного облака в кристалле с понижением температуры
а) кристаллическая решетка с металлической связью Т>> Тхр
б) кристаллическая решетка с ковалентной и металлической составляющей Т>Тхр
в) кристаллическая решетка с ионной или ковалентной связью Т<Тхр
Количество уровней, которые могут быть заняты электронами, уменьшается. Как следствие, меньше электронов участвуют в создании связи кристалла. Происходит вырождение металлической связи в ковалентную, появляются провалы пластичности и хладноломкость.
Представленное описание хладноломкости достаточно хорошо согласуется с имеющимися теориями хладноломкости: со схемой Иофе – Давиденкова, где основным соотношением является Тхр=f(σкрист/σхр); со схемой Джеффрика – Арчера, где переход к хрупкости определяется соотношением: σ, δ=f(квазиаморфн/квазикристалл); с кластерной теорией Ф=f1Ф1+f2Ф2, где Ф – суммарное свойство, Ф1,Ф2 – свойство кристаллической и бесструктурной фазы, f1, f2 – мольные доли; с классификацией Б.Б. Гуляева, где твердый и жидкий раствор представляются как сумма расслоений жидкого раствора как классического бесструктурного вещества и твердого раствора, как вещества со сложной структурой; со схемой В.И. Ивановой, где разрушение представляется как процесс образования квазиаморфных областей в кристалле и их разрушений.
Так, при разрушении аустенитных сталей в связи с их низкой теплопроводностью в них происходит значительный разогрев с увеличением доли «теплового» члена уравнения энергии. Это резко увеличивает пластичность и переход кристаллической решетки в квазиаморфное состояние. Ничего подобного не происходит в ферритных сталях, поскольку они обладают высокой теплопроводностью и при низких температурах тепло быстро рассеивается. Это не дает возможности повысить эффективность работы «теплового» члена в уравнении энергии и стали разрушаются хрупко.
Учитывая прямую связь электронного строения расположением металлов в периодической системе Д.И. Менделеева, можно сказать, что хладноломкость относится к числу фундаментальных свойств элементов. Отметим, что не все механические свойства металлов, учитываемые в технических условиях, вписываются в Периодическую систему.
Схема появления хладноломкости
Таким образом, рождение хладноломкости на атомном уровне происходит в следующем порядке:
- С понижением температуры уменьшается тепловое колебание электронов. В результате этого происходит ужесточение сферы Ферми, и ее радиус становится меньше. При этом уменьшается электронная концентрация, и меньшее количество электронов остается в коллективизированном состоянии, обеспечивающих металлическую связь в кристаллической решетке.
- Происходит изменение соотношения металлической связи и других видов связей (ковалентной, ионной и пр.) в пользу ковалентных связей. Поскольку свойства высокой пластичности в больше степени обеспечиваются металлической связью (например, залечивание микроразрушений кристаллической решетки, происходящих даже на уровне элементарной ячейки), то уменьшение коллективных электронов или сужение сферы Ферми, зон Бриллюэна по кристаллу и разделение их для металлов, имеющих перекрытые зоны, приводит к превалированию ионной и ковалентной связи. Это наиболее сильно выражено в областях, имеющих искаженную кристаллическую решетку, близкую к квазиаморфному состоянию. При этом должны выполняться соотношения:
Тхр/Тпл = f(Uкрист/U отд атомов) = f(Nколлект эл/Nполн) =f(rфТхр/rфТпл) (5)
ВЫВОДЫ И РЕКОМЕНДАЦИИ
-Переход из пластичного состояния в хрупкое хорошо описывается уменьшением доли связи коллективизированных электронов и переходом их в более жесткую ковалентную связь.
- Дальнейший поиск сплавов с низкой температурой вязко-пластичного перехода должен основываться на определении механических свойств, как дочерних свойств периодической системы Д.И. Менделеева и определения особенностей перехода каждого элемента химсостава стали и сплава в хрупкое состояние при данных условиях.
- Выбор легирующих элементов должен проводиться по условиям их собственной нехладноломкости, где: Тхр эл < 0,1 Тпл эл; легирующий элемент образует твердый раствор с матрицей сплава, обеспечивает значительный вклад в долю коллективизированных электронов и экономически целесообразен. Собственно поиск легирующих элементов необходимо вести в направлении изыскания элементов, расширяющих зоны коллективных электронов, имеющих перекрытые зоны 3d-4f.
-Фазовый состав нехладноломких сталей желательно подбирать таким образом, чтобы обеспечивать полноту реализации эффекта «теплового» члена уравнения энергии, в частности, на основе аустенита.
Литература:
1.Р. Спроул. Современная физика, М., Наука, 1974 г.
2.Пресняков А.А., Хладноломкость. Алма-Ата, Наука, 1967, 199 стр.
3.Горобченко С.Л., Кривцов Ю.С., Гуляев Б.Б. О связи хладноломкости с периодической системой Д.И. Менделеева, Л., ЛГУ, 1989., деп.
4.Горобченко С.Л., Кривцов Ю.С., О хладноломкости литых сталей и сплавов, CD ROM, Санкт-Петербург, 2013.
5.Ермаков С.С. Физика металлов, ЛПИ, 1975